2025年5月底,Rocket Pharmaceuticals公司正在进行的Danon病基因疗法RP-A501关键2期临床试验因一名患者不幸去世而不得不暂停。在降低药物剂量并更改免疫调节剂的使用方案后,该公司已获得FDA的许可,允许试验继续进行。
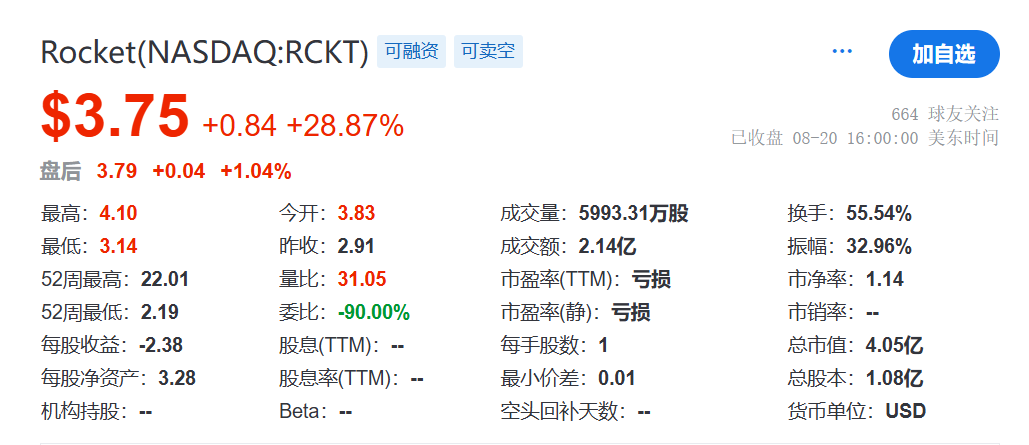
2025年8月20日,致力于为高需求罕见病开发可持续的基因疗法管线的Rocket Pharmaceuticals宣布,美国食品药品监督管理局(FDA)已解除对其关键性2期试验RP-A501(用于治疗Danon病)的临床暂停。
消息发布后,Rocket股价大涨28.87%。
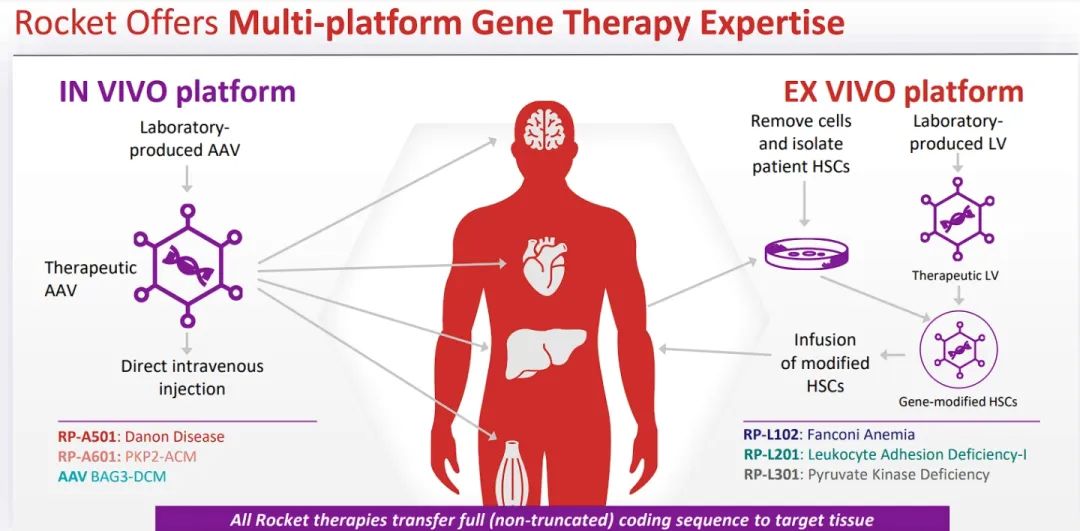
RP-A501是Rocket公司开发的一种基因疗法,旨在通过AAV9载体将功能性LAMP2B基因导入心脏细胞,从而恢复心脏功能。Danon病是一种罕见的X连锁遗传性疾病,由LAMP2基因突变引起,导致心脏和其他组织中自噬体和糖原的积累,最终引发心力衰竭。该病通常导致男性患者在20岁左右、女性患者在40岁左右死亡。
RP-A501 2期关键试验是一项全球、单臂、多中心研究,旨在评估RP-A501在12名Danon病患者中的疗效和安全性。试验以儿科安全性导入期(n=2)启动,随后以6.7×10 GC/kg的剂量共治疗了6例患者。
FDA在来函中确认,Rocket已妥善解决临床暂停期间提出的所有问题,并批准该关键研究首先以调整后的剂量——3.8 × 10 GC/kg 的RP-A501重启,首批治疗3例患者,采取序贯给药,每例之间至少间隔4周。该剂量位于1期研究中显示有效性的多个生物标志物、超声心动图和临床终点所对应的较低剂量区间,被认为最有可能同时实现1期低剂量组观察到的安全性与疗效。
此外,Rocket将与研究者合作,实施一套更贴近1期儿科队列实际使用的免疫调节方案:取消C3补体抑制剂的预防性使用,继续使用西罗莫司、利妥昔单抗及类固醇;并在出现即将发生补体激活的指标时,设定更低的阈值以启动C5抑制剂(依库珠单抗)治疗。
截至目前,已有6名Danon病患者在RP-A501的2期研究中接受治疗。待后续3名患者数据审阅完毕后,将公布更多研究进展。
参考资料:公司公告
网上配资的平台,杠杆炒股配资平台,我要配资网官网网址提示:文章来自网络,不代表本站观点。
- 上一篇:配资优选说不准还能捞到一官半职
- 下一篇:配资服务融资融券余额5437.94万元